Gonadotropina umană este un hormon care este produs. Hormoni gonadotropi. Influența nivelului TSH asupra zonei genitale feminine
Hormonii umani sunt substanțe organice de diferite structuri. În funcție de semnificația lor fiziologică, acestea sunt împărțite în două grupe: așa-numiții hormoni de pornire care stimulează activitatea glandelor endocrine (hormonii hipotalamusului și hipofizei) și hormoni-executori care afectează direct anumite funcții ale corpului.
Hormoni gonadotropi hipofizari
Stimulează activitatea ovarelor. Au fost identificați trei astfel de hormoni: hormonul foliculostimulant (FSH), care promovează dezvoltarea foliculilor ovarieni; luteinizarea (LH), care determină luteinizarea foliculară; luteotrop (LTG), care susține funcția corpului galben în timpul ciclului menstrual și are efect lactotrop.
FSH și LH sunt apropiate unele de altele în structura chimică (ambele sunt glicoproteine), precum și în proprietățile fizico-chimice. Acest lucru face foarte dificilă izolarea lor de glanda pituitară în forma lor pură. Cu toate acestea, similitudinea structurală a FSH și LH joacă, evident, un rol special, deoarece reglarea activității ovariene se realizează odată cu acțiunea comună a acestor hormoni.
FSH (greutatea moleculară relativă 30.000) formează mici bazofile rotunjite situate în regiunile periferice ale glandei pituitare anterioare. Nucleul acestor celule are o formă neregulată, iar citoplasma conține un număr mare de boabe mari de glicoproteine.
LH (greutatea moleculară relativă 30.000) este format din bazofile situate în partea centrală a lobului anterior. Nucleii lor au, de asemenea, o formă neregulată; citoplasma conține multe granule bazofile. Moleculele FSH și LH conțin o componentă glucidică, care include hexoză, fructoză, hexozamină și acid sialic.
Activitatea fiziologică a ambilor hormoni este determinată de prezența legăturilor disulfidice și de un conținut ridicat de cistină și cisteină.
Deoarece FSH și LH sunt sinergice și aproape toate efectele biologice ale acțiunii lor - dezvoltarea foliculilor, ovulația, secreția hormonilor sexuali - se efectuează cu eliberare articulară, este rațional să se ia în considerare efectul complex al acestora asupra organelor și sistemelor.
Conform datelor actuale, preparatele FSH foarte purificate nu stimulează dezvoltarea foliculilor din ovar, în timp ce un amestec mic de LH determină creșterea și maturarea acestora. Callantie (1965) a reușit să arate că efectul specific al FSH asupra ovarelor este de a stimula sinteza ADN-ului în nucleele celulelor foliculare. Studii mai recente au demonstrat că acest lucru necesită acțiunea simultană a estrogenilor (Mapgoe și colab., 1972; Reter și colab., 1972).
Se știe că gonadotropinele cresc greutatea ovariană și, prin urmare, sinteza proteinelor. Ele sporesc activitatea unui număr de enzime implicate în metabolismul proteinelor și glucidelor.
Concentrația de FSH și LH în glanda pituitară crește treptat spre debutul pubertății. Activitatea biologică a hormonului gonadotrop la persoanele de vârste diferite nu este aceeași. Deci, FSH excretat din urina fetelor este mult mai activ decât excretat din urina femeilor adulte și a femeilor care au venit.
În timpul sarcinii, un alt hormon gonadotrop se formează în placentă - goiadotropină corionică (CG). Are un efect biologic similar cu hormonii gonadotropi ai glandei pituitare. Secreția gonadotropinelor de către glanda pituitară este slăbită în timpul sarcinii.
Pe lângă efectul specific asupra ovarelor, hormonii gonadotropi au un efect pronunțat asupra multor procese din organism. S-a constatat că atât CG, cât și LH cresc activitatea fibrinolitică a sângelui (Ch.S. Guseinov și colab., 1967). Prezența gonadotropinelor în preparatele de albumină produse le face eficiente în clinică pentru tratamentul alergiilor și bolilor cu o componentă imunologică.
Odată cu introducerea hormonilor gonadotropi, excitabilitatea diferitelor părți ale sistemului nervos se schimbă. Acestea au un efect trofic pozitiv și accelerează vindecarea ulcerelor gastrice experimentale la animale.
LTG (greutate moleculară relativă 24.000-26.000) este format din acidofili pituitari. Citoplasma acestor celule conține multe boabe care se colorează în roșu cu carmin.
Conform structurii sale chimice, LTG este o proteină simplă. Principalul său efect biologic este activarea formării laptelui în timpul alăptării la unele specii de animale și la oameni. În plus, hormonul susține funcția endocrină a corpului galben.
Antigonadotropine
Când hormonii gonadotropi izolați din serul sau glanda pituitară a animalelor sunt introduși în corpul uman, în sânge apar anticorpi antigonadotropi specifici. Ele neutralizează acțiunea hormonului injectat.
Studiile efectuate de Stevens și Crystle (1973) au arătat că, atunci când se administrează gonadotropină corionică, în organism se formează anticorpi care reacționează cu LH. Evident, acest lucru se datorează apropierii structurilor chimice ale CG și LH. În preparatele insuficient purificate izolate din urină sau țesut hipofizar, pot fi prezente și antigonadotropine (ON Savchenko, 1967). Natura acestor substanțe nu a fost încă clarificată. Se știe că, spre deosebire de hormonii gonadotropi, aceștia sunt stabili termic.
Hormoni sexuali
Grupul de hormoni sexuali („hormonii reproducerii”) aparține așa-numiților hormoni-executori, care afectează organele genitale, precum și întregul organism. Se formează în ovare, în cantități mai mici în cortexul suprarenal. În timpul sarcinii, placenta este sursa hormonilor sexuali.
Prin acțiune și locul de formare, acestea se împart în: estrogeni, provocând estrus (estrus) sau keratinizarea epiteliului vaginal la animale; gestageni sau hormoni ai corpului galben, a căror principală proprietate fiziologică este de a stimula procesele care asigură implantarea oului în curs de dezvoltare și dezvoltarea sarcinii; androgeni sau hormoni sexuali masculini care au efect virilizant.
Pe lângă aceste substanțe, ovarele produc un alt hormon - relaxina, care determină relaxarea ligamentelor articulației pubiene în timpul nașterii, precum și înmuierea colului uterin și extinderea canalului cervical. Cu toate acestea, rolul acestui hormon în organism nu este bine înțeles.
Estrogenii și gestagenele sunt hormoni sexuali feminini. Acestea au un efect specific în primul rând asupra aparatului genital, precum și asupra glandelor mamare. Organul cel mai sensibil la acțiunea hormonului se numește organ țintă. Pentru hormonii sexuali, țintele sunt uterul, vaginul, trompele uterine și ovarul. În ceea ce privește structura chimică, toți hormonii sexuali, cu excepția relaxinei, sunt steroizi. Acestea sunt substanțe care au structura ciclopentanfenantrenului și sunt construite după o schemă generală. Inelele care alcătuiesc scheletul steroizilor sunt de obicei notate cu literele A, B, C și D.
Ordinea numerotării atomilor de carbon din seria compușilor steroizi s-a dezvoltat istoric în cursul cercetărilor lor. Atomii de carbon ai inelelor A, B și D sunt numerotați în sens invers acelor de ceasornic, atomii inelului C sunt numerotați în direcția sa.
Estrogeni

Aceștia sunt cei mai importanți hormoni sexuali feminini. Cele mai multe dintre ele se formează în ovare - în celulele interstițiale și căptușeala interioară a foliculilor. La femeile care nu sunt însărcinate, o anumită cantitate de estrogen este produsă și în cortexul suprarenal.
Principalii estrogeni sunt estradiolul, estrona și estriolul. În plus, un număr de alți hormoni estrogeni au fost izolați din fluidele biologice ale corpului uman, care sunt considerați ca produse metabolice ale celor trei estrogeni principali.
Proprietatea comună a tuturor acestor substanțe este capacitatea de a induce estru la animale. Prin urmare, atunci când se evaluează activitatea unui hormon, se ia în considerare cantitatea minimă a acestuia care provoacă estru.
Pentru a determina activitatea hormonilor sexuali feminini, se folosește metoda Allen și Doisy. Constă în administrarea de extracte ovariene sau de diverse cantități de substanțe hormonale studiate la animale castrate (șoareci sau șobolani), ceea ce le determină să se încălzească. Un tampon luat în timpul estrului conține un număr mare de celule keratinizante. Cea mai mică cantitate dintr-o substanță, cu introducerea căreia celulele keratinizante pot fi detectate la 70% din șoarecii castrați experimentali, se numește unitate de șoarece.
Conform unui acord internațional încheiat în 1939, estrona cristalină este considerată medicamentul standard.
IN Nazarov și LD Bergelson (1955), injectarea șoarecilor cu hormoni estrogeni subcutanat, a determinat că cea mai mică doză activă de estronă este de 0,7 μg, estradio-la-176 - 0,1 și estriol - 10 μg. Prin urmare, conform testului Allen și Doisy, estradiolul este cel mai activ estrogen, iar estriolul este cel mai puțin activ.
Activitatea hormonului depinde în mare măsură de modul de administrare. Astfel, estriolul, atunci când este administrat subcutanat, acționează mai slab, iar atunci când este administrat oral, este mai puternic decât estrona.
Activitatea biologică a celor trei estrogeni principali este diferită și fiecare dintre ei are un efect diferit asupra organelor țintă - uter și vagin. Deci, dacă estradiolul este mai activ decât estriolul și estrona conform testului Allen și Doisy, atunci estriolul s-a dovedit a fi cel mai activ conform unui alt test: o creștere a greutății uterului șobolanilor imaturi. În consecință, endometrul este cel mai sensibil la estradiol, iar mușchiul uterin este cel mai sensibil la estriol. Dozele mici de estriol au un efect semnificativ asupra țesuturilor vaginale și a canalului cervical. Când este introdus în epiteliul acestor organe, mucopolizaharidele neutre se formează mai intens decât sub acțiunea estronei și estradiolului. Endometrul răspunde doar la cantități mari de estriol.
În prezent, au fost sintetizate peste 100 de medicamente care au proprietăți estrogenice pronunțate, dar nu au o structură steroidică. Activitatea estrogenică a acestor substanțe este mai mare decât cea a hormonilor steroizi, în plus, acțiunea lor este identică atât pentru administrare orală, cât și parenterală.
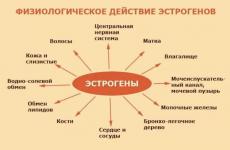
Principala proprietate biologică a tuturor estrogenilor, atât steroizi, cât și nesteroidieni, este capacitatea de a avea un efect specific asupra organelor genitale feminine și de a stimula dezvoltarea caracteristicilor sexuale secundare.
Estrogenii provoacă hipertrofie și hiperplazie a endometrului și miometrului. Chiar și o singură administrare a acestor hormoni afectează vasele uterului, stimulând secreția de histamină și serotonină, care cresc permeabilitatea capilarelor uterine, ceea ce duce la o retenție de sodiu și apă în țesuturi. Epiteliul cilindric al colului uterin devine multistratificat sub influența estrogenilor, epiteliul glandelor tubulare începe să secrete o secreție mucoasă cu vâscozitate scăzută, ca urmare a căreia, cu o creștere a secreției de estrogen, trecerea spermatozoizilor în cavitatea uterină este facilitată.
Sub influența estrogenilor, epiteliul vaginal suferă, de asemenea, modificări caracteristice. Straturile de celule se îngroașă, glicogenul este depus în ele, ceea ce contribuie la reproducerea bastoanelor de Dederlein.
Estrogenii contribuie la dezvoltarea sistemului excretor al glandelor mamare, precum și la hipertrofia stromei glandei. Un interes considerabil este problema efectului estrogenilor asupra apariției cancerului de sân. Deși experimentele pe animale nu au arătat o dependență strictă a dezvoltării cancerului de doza de estrogeni administrați, relația dintre creșterea conținutului de estrogeni (persistența foliculului, tumoarea ovariană etc.) cu dezvoltarea fibrelor chistice s-a dovedit mastopatia. O creștere a activității mitotice a epiteliului glandelor mamare sub influența estrogenilor a fost demonstrată în mod convingător (S. S. Laguchev, 1970).
Introducerea unor doze mari de estrogeni, ca și alți hormoni produși de glandele endocrine periferice, inhibă secreția hormonilor hipofizari și hipotalamici de pornire, care sunt direct legați de producția de estrogeni - FSH și LH.
Hormonii estrogeni afectează nu numai organele țintă, ci și întregul corp, acest lucru trebuie luat în considerare atunci când se prescrie terapia hormonală.
Sub influența estrogenilor, sodiul, apa și azotul sunt reținute în organism. În același timp, debitul de urină scade de obicei.
Efectul estrogenilor asupra metabolismului lipidic este clar exprimat. Există o relație între funcția ovariană și apariția aterosclerozei. Când ovarele sunt îndepărtate, atât în clinică, cât și în experiment, se observă o creștere a conținutului de colesterol din sânge. Prin urmare, estrogenii sunt utilizați în tratamentul aterosclerozei.
Dozele fiziologice de estrogeni stimulează funcția sistemului reticuloendotelial, crescând producția de anticorpi și activitatea fagocitelor. Drept urmare, rezistența organismului la infecții crește.
După o singură injecție de estrogeni, vasele creierului se extind, posibil datorită eliberării de acetilcolină. De asemenea, s-a constatat (Goodrich, Wood, 1966) că estradiolul crește elasticitatea venelor periferice. Acest lucru duce la o scădere a vitezei fluxului de sânge în ele. Administrarea pe termen lung de estrogeni, pe de altă parte, crește tensiunea arterială. Estrogenii au un efect clar asupra hematopoiezei. Acest lucru explică numărul mai mic de eritrocite la femele decât la masculi (S. I. Ryabov, 1963).
Estrogenii determină într-o anumită măsură înălțimea și greutatea corpului. A fost sugerat un rol semnificativ al estrogenilor în reglarea diviziunii celulare, dar datele despre această problemă sunt contradictorii. Se știe că odată cu introducerea unor doze mari de estrogeni, focarele de proliferare apar în organism, dobândind uneori un caracter blasto-matos. Pe de altă parte, există dovezi ale efectului inhibitor al estrogenilor asupra creșterii neoplasmelor, în special asupra creșterii tumorilor de prostată. Hertz (1967), în analiza materialului despre rolul hormonilor steroizi în etiologia și patogeneza cancerului, a concluzionat că studiile clinice nu pot dovedi capacitatea estrogenilor de a induce neoplasme.
Estrogenii afectează aproape toate organele endocrine. Efectul lor depinde în mare măsură de doză. Deci, dozele mici și medii stimulează dezvoltarea ovarelor și maturarea foliculilor, cele mari suprimă ovulația și duc la persistența foliculilor, iar dozele foarte mari provoacă procese atrofice în ovare (V.E. Liivrand, V.A.Kask, 1973). Estrogenii au o mare influență asupra hipofizei anterioare (adenohipofiză). Cantități mici dintre acestea stimulează formarea hormonilor în glandă, iar cele mari, dimpotrivă, inhibă activitatea acestuia. Hormonii estrogenici blochează formarea hormonului de creștere. Această circumstanță trebuie reținută atunci când se prescriu medicamente estrogenice pacienților de vârstă pubertară și prepubertală.
Efectul estrogenilor afectează și funcția glandei tiroide. Deși datele despre natura acestui efect sunt contradictorii, majoritatea autorilor remarcă efectul stimulant al dozelor mici de hormoni și efectul de blocare al celor mari (NK Gridneva, NG Dorosheva, 1973).
Estrogenii stimulează cortexul suprarenal: sub influența lor, masa glandelor suprarenale crește după castrare și conținutul de corticosteroizi din sânge crește. Sub influența estrogenilor, apare atrofia glandei timusului.
Deși efectele estrogenilor ovarieni și ale estrogenilor nesteroidieni asupra ambelor organe țintă și a corpului sunt similare, există unele diferențe care ar trebui luate în considerare atunci când se alege terapia hormonală rațională. Deci, medicamentele steroizi au un efect mai ușor și au mai puține efecte secundare. Evident, acest lucru se datorează faptului că estrogenii naturali sunt eliminați mai repede din corp, fiind inactivați în ficat. În plus, estrogenii nesteroidieni au un efect mai pronunțat asupra celulelor hepatice, prin urmare, dacă funcția sa este afectată, utilizarea lor ar trebui să fie limitată.
Antiestrogeni... Există o serie de substanțe, a căror acțiune asupra organelor genitale este opusă acțiunii estrogenilor, adică sunt antagoniștii lor. Aceste substanțe pot fi împărțite în trei grupe: tipuri de androgeni, care inhibă creșterea uterului și reduc greutatea ovarelor (acest grup include și hormoni ai cortexului suprarenal, care au un efect similar); substanțe asemănătoare ca structură cu estrogenii sintetici precum sinestrolul, având un efect estrogen slab, dar suprimând efectul estrogenilor mai puternici produși în organism (dimetilstil-bestrol, floretin etc.); substanțe care nu sunt steroizi și nu au nicio asemănare structurală cu estrogenii sintetici.
Gestagene

La fel ca estrogenii, sunt hormoni sexuali feminini. Principala este progesteronul. Este sintetizat în corpul galben al ovarelor, precum și în placentă și cortexul suprarenal. În corpul galben se formează și 17-hidroxiprogesteronă.
La fel ca estrogenii, are un efect specific în primul rând asupra organelor genitale. Unele dintre efectele progesteronului sunt opuse celor ale estrogenilor. În cazul fertilizării, acest hormon suprimă ovulația, menține condițiile din uter necesare dezvoltării fătului și previne contracțiile acestuia. Efectul antagonist al progesteronului se manifestă și în suprimarea keratinizării epiteliului vaginal cauzată de estrogeni. Dozele mari de progesteron reduc efectul proliferativ al estrogenilor asupra endometrului.
Cu toate acestea, relația dintre estrogeni și progesteron este mult mai complexă decât cele antagonice. Acești hormoni sunt adesea sinergici. Efectul biologic al progesteronului apare în majoritatea cazurilor după stimularea estrogenică. Împreună cu ele, gestagenii provoacă modificări ale glandelor mamare: dacă estrogenii prelungesc și îngroșează conductele, atunci progesteronul îmbunătățește dezvoltarea alveolelor. Sub acțiunea gestagenelor asupra uterului, stimulate anterior de estrogeni, s-a remarcat proliferarea și secreția glandelor endometriale; modificări apar și în celulele stromei - crește dimensiunea nucleilor, crește conținutul unor enzime și glicoproteine. Progesteronul este necesar pentru menținerea sarcinii, cu toate acestea, îndepărtarea corpului galben determină întreruperea sarcinii doar în stadiile incipiente. Ulterior, progesteronul este produs în placentă.
Pe lângă efectul specific asupra organelor țintă, gestagenele afectează multe procese din corp. Deci, progesteronul reține apă și sare, crește conținutul de azot în urină; crește temperatura corpului, ceea ce creează condiții optime pentru dezvoltarea unui ovul fertilizat; are un sedativ direct și, în doze mari, un efect narcotic.
Efectul hipotensiv al gestagenelor a fost de asemenea descris atât în clinică, cât și în hipertensiunea experimentală (Armstrong, 1959). Gestagenele cresc secreția de suc gastric și inhibă secreția de bilă.
Efectul progesteronului asupra organelor endocrine, precum cel al estrogenilor, este dependent de doză. Deci, cantități mici din acesta stimulează activitatea glandei pituitare, crescând secreția de hormoni gonadotropi, iar cantități mari blochează producția lor, prevenind astfel maturarea foliculului și ovulația.
Proprietatea gestagenelor de a inhiba ovulația, provocând un efect contraceptiv, a fost stabilită de Haberland în 1921. El a descoperit infertilitatea temporară la animale după implantarea corpului galben sau a țesutului placentei.
În plus față de acțiunea antigonadotropă, progesteronul afectează direct ovarul, reducând dimensiunea acestuia și inhibând dezvoltarea foliculilor. Administrarea prelungită de gestageni în organism duce la o scădere a funcției glandelor suprarenale.
Influențând glanda tiroidă, gestagenele determină o creștere a cantității de iod legat de proteine și o creștere a capacității de legare a tiroxinei a globulinelor.
În prezent, a fost sintetizat un număr semnificativ de steroizi cu efect gestagenic, care este mai puternic decât efectul progesteronului: acetat de clormadinonă, cel mai puternic progestogen, care are o activitate de 100 de ori mai mare decât progesteronul și are un efect nesemnificativ asupra gonadotropului funcția glandei pituitare; acetat de medroxi-progesteron - de 15 ori mai activ decât progesteronul în acțiunea sa asupra aparatului de reproducere și de 80 de ori mai activ în acțiunea sa antigonadotropă etc.
Androgeni

Androgenii sunt hormoni sexuali masculini. Formată atât în corpul masculin, cât și în cel feminin. La femei, acestea sunt sintetizate în principal în zona reticulară a cortexului suprarenal. În cantități mici, acești hormoni sunt produși și în ovare. Secreția ovariană de androgeni crește brusc în unele condiții patologice - ovare polichistice și mai ales în arhenoblastoame (KD Smirnova, 1969). Ovarele produc în principal androstendionă, testosteron și epitestosteron. Ultimii doi hormoni sunt sintetizați în cantități semnificative în tumori. Activitatea biologică a androgenilor este diferită. Unitatea internațională a activității lor biologice este activitatea a 100 μg de androsteron, care este echivalentă cu activitatea a 15 μg de testosteron. La fel ca toți hormonii sexuali, androgenii afectează în principal organele genitale, iar efectul lor depinde de doză.
Androgenii stimulează creșterea clitorisului, provoacă hipertrofia labiilor majore și atrofia labiilor majore și afectează, de asemenea, uterul și vaginul.
Este caracteristic faptul că efectul androgenilor asupra uterului se efectuează numai la femeile cu ovare funcționale, adică pe fondul unei anumite saturații estrogenice. În același timp, doze mici de hormoni androgenici provoacă modificări pregravidice în endometru, iar doze mari provoacă atrofie. În miometru, odată cu introducerea unor doze mari, fluxul sanguin scade, se dezvoltă fibroza și hiperplazia chistic-glandulară.
Pe vagin, androgenii au un efect similar gestagenilor, adică inhibă proliferarea membranei mucoase cauzată de hormonii estrogenici. Când funcția ovariană este oprită, androgenii administrați în doze mari determină o oarecare proliferare a mucoasei vaginale. Evident, la fel ca gestagenii, androgenii pot, în funcție de doză, să acționeze ca sinergici sau antagoniști ai hormonilor estrogeni. Astfel, cantități mici de androgeni sporesc efectul estrogenilor asupra uterului și vaginului animalelor castrate, iar dozele mari, dimpotrivă, reduc efectul hormonilor estrogeni.
Androgenii inhibă formarea laptelui în glanda mamară, inhibând secreția acestuia la mamele care alăptează. Dozele mici de androgeni stimulează formarea hormonilor gonadotropi de către glanda pituitară, care la rândul său activează maturarea foliculilor din ovare, iar dozele mari blochează funcția glandei pituitare. Acest efect și-a găsit aplicarea în tratamentul cancerului de sân, când doze mari de testosteron determină o scădere a secreției de hormoni gonadotropi ai glandei pituitare și modificări atrofice în ovare (Ya.M. Bruskin,
1969).
Androgenii au un efect pronunțat asupra glandelor suprarenale. Studiile experimentale efectuate de mulți autori au arătat că administrarea pe termen lung a testosteronului duce la o scădere a funcției cortexului suprarenal (Mc Carty și colab., 1966; Telegry și colab., 1967). BV Epshtein (1968), DE Yankelevich și M. 3. Yurchenko (1969) au observat suprimarea funcției cortexului suprarenalial atunci când se utilizează medicamente androgene în clinică.
Evident, efectul androgenilor asupra stării funcționale a glandelor suprarenale este, de asemenea, dependent de doză. Conform lui I. N. Efimov (1968), Roy și coautori (1969), doze mici din acești hormoni reduc funcția glandelor suprarenale, iar dozele mari o stimulează. În același timp, Kitay și colab. (1966) dau rezultate opuse.
Androgenii stimulează funcția insulelor Langerhans din pancreas, cu un anumit efect antidiabetic.
În mod normal, femeile produc în corpul lor mai puțini androgeni decât bărbații. Cu toate acestea, cu tumorile hormonale active, precum și cu cele polichistice (), ovarele pot produce un număr mare de compuși androgenici, ceea ce duce la apariția caracteristicilor sexuale masculine secundare la femei.
Același lucru se poate observa și pentru androgeni sintetizați de cortexul suprarenal al femeilor. Deci, dacă în mod normal se formează o cantitate mică de hormon androgen dehidroepiandrosteron în zona reticulară a cortexului suprarenal, atunci cu hiperfuncție a glandei suprarenale și cu atât mai mult cu tumora sa, sunt eliberați mulți androgeni, ceea ce determină virilizarea.
Pe lângă efectul pronunțat asupra organelor genitale, androgenii sunt implicați în reglarea metabolismului proteinelor, grăsimilor și mineralelor.
Efectul stimulator al androgenilor asupra sintezei proteinelor este indicativ în special. Acest așa-numit efect anabolic se datorează unei creșteri a sintezei proteinelor asupra ARN-ului ribozomal, ceea ce duce la retenția de azot. Creșterea sintezei proteinelor are loc cel mai intens în țesutul muscular. Acest efect anabolic al androgenilor explică dezvoltarea musculară mai puternică la bărbați decât la femei (Zachmann și colab., 1966).
În plus față de retenția de azot în organism, androgenii provoacă acumularea de fosfor și potasiu, care sunt componente ale proteinelor tisulare, precum și reținerea de sodiu și clor și reduc excreția de uree.
Androgenii accelerează creșterea osoasă și osificarea cartilajului epifizar. De asemenea, au un efect asupra hematopoiezei, crescând numărul de celule roșii din sânge și hemoglobină.
Proprietatea androgenilor de a crește sinteza proteinelor a dat naștere la crearea unui întreg grup de hormoni steroizi anabolizanți. Astfel de substanțe sunt utilizate pe scară largă în clinică pentru tratamentul pacienților după intervenții chirurgicale, cu epuizare etc. Deoarece testosteronul și androsteronul au atât efect androgen, cât și anabolic, care împiedică utilizarea acestor hormoni la femei, în prezent sunt sintetizate medicamente care au un efect androgen pronunțat slab și puternic efect anabolic. Acești hormoni sunt 1 / -etil-19-nortestosteron (nilevar, noretan-drolon), care are o activitate androgenică de 16 ori mai mică decât testosteronul (Fig. 12), nerobol (dianabol), nerobolil (durabolin), retabolil norboleton, oxandrolon etc. .
Antiandrogeni... Sunt folosite pentru tratarea acneei vulgare, hirsutismului, fetelor etc. Hammerstein (1973) descrie unul dintre medicamentele antiandrogenice extrem de eficiente - acetat de ciproteronă, care, pe lângă acțiunea antiandrogenă, are și proprietăți contraceptive. Utilizarea acestuia duce la o scădere accentuată a conținutului de progesteron în plasma sanguină.
Mecanismul de acțiune al hormonilor steroizi
În ciuda faptului că efectul hormonilor steroizi asupra diferitelor aspecte ale metabolismului este bine cunoscut, mecanismul acțiunii lor la nivel celular și molecular nu este bine înțeles. Succesul în această direcție a fost obținut în studiul proprietăților fizice ale hormonilor steroizi în legătură cu structura lor chimică.
Deci, dacă ne imaginăm o moleculă de steroizi situată în planul unei foi de hârtie, atunci grupurile unghiulare de metal sunt plasate deasupra acestui plan. Grupurile care sunt proiectate în aceeași direcție se numesc cis, iar în direcția opusă, trans. La scrierea formulei structurale, aceste proiecții sunt descrise prin linii solide și, respectiv, întrerupte. Aceste diferențe spațiale conferă moleculelor de steroizi proprietăți chimice și biologice diferite.
Deoarece o modificare a aranjamentului spațial al unei molecule de steroizi duce la o schimbare a activității biologice, este firesc să concluzionăm că acțiunea farmacologică a steroizilor este strâns legată de structura lor chimică. Varietatea efectelor acțiunii acestor hormoni asupra corpului, aparent, este posibilă datorită prezenței mecanismelor comune de acțiune a acestora în celule. Descifrarea acestor mecanisme este esența răspunsului farmacologic primar cauzat de steroizi.
Cu toate acestea, selectivitatea acțiunii hormonilor asupra diferitelor organe nu depinde de structura lor chimică. Când circulă în sânge, acestea ajung la celulele tuturor organelor și țesuturilor și se acumulează numai în anumite organe țintă, în celulele cărora există substanțe proteice speciale - receptori care intră într-o legătură chimică cu hormonul. În prezent, au fost studiate greutatea lor moleculară și alte caracteristici, iar numărul de molecule receptor în celulă și capacitatea legăturilor care asigură interacțiunea lor cu steroizii au fost calculate. Deci, o celulă a epiteliului uterin conține 2000-2500 de receptori care leagă estradiolul.
Astfel, interacțiunea unui hormon steroid cu o moleculă de receptor dintr-o celulă este una dintre condițiile pentru mecanismul molecular al modificărilor biochimice complexe ulterioare ale organelor și țesuturilor.
Există mai multe ipoteze despre posibilul mecanism de acțiune al steroizilor asupra celulei (AM Utevsky, 1965): hormonii acționează pe suprafața celulei, modificând permeabilitatea membranei sale; interacționează cu sistemele enzimatice; controlează activitatea genelor.
Deoarece funcțiile membranelor celulare sunt indisolubil legate de acțiunea enzimelor „încorporate” în aceste membrane, iar aparatul informației genetice funcționează conform principiului „o genă - o enzimă”, atunci când se analizează punctele de aplicare a acțiunii. a oricărui hormon steroid, efectul lor asupra enzimelor izolate iese în prim plan și a sistemelor enzimatice.
Din acest punct de vedere, mecanismul de acțiune al estrogenilor este cel mai bine studiat (Gorski și colab., 1965; O.I. Epifanova, 1965; P.V. Sergeev, R.D.Seyfulla, A.I. Maisky, 1971; S.S. La-Guchev, 1975). Potrivit lui Gorski și colegilor săi, interacțiunea moleculară a estrogenilor cu organele țintă are loc în trei etape, iar influența lor asupra aparatului genetic al celulei este un efect ulterior al acțiunii. În primul rând, molecula de estrogen se leagă stereospecific de molecula receptorului din celulă, apoi se modifică activitatea biologică a moleculei receptorului, iar în etapa finală crește sinteza ARN, glucoză, fosfolipide și proteine.
Mulți hormoni și, în principal, hormoni declanșatori (hormoni ai hipofizei și hipotalamusului), care acționează asupra celulei, activează enzima adenilciclază, localizată în membrana celulară, asociată cu un receptor specific pentru fiecare hormon. Aceasta crește sau scade cantitatea de acid monofosforic 3 ", 5" -adenozină ciclic (3 ", 5" -AMP), care la rândul său activează elemente intracelulare.
Astfel, AMP de 3 ", 5" este, ca să spunem așa, un mediator intracelular, care asigură transmiterea influenței hormonului asupra sistemelor enzimatice intracelulare. Există dovezi că hormonii steroizi acționează și indirect prin 3 ", 5" AMP.
Biosinteza hormonilor steroizi sexuali are caracteristici comune, iar etapele sale inițiale, care se desfășoară atât în ovare, cât și în glandele suprarenale și testicule, sunt identice.
Pregnenolonă, care are o activitate hormonală slabă, conform conceptelor moderne, este principala substanță din care hormonii se formează ulterior în diferite organe endocrine. În această secvență, pregnenolona este sintetizată în glandele suprarenale, testicule, foliculi, corpul galben și stroma ovariană (Hall, Koritz, 1964; Ryan, Smith, 1965; Ryan, Petro, 1966). Aceste etape în conversia colesterolului în pregnenolonă sunt de un interes deosebit, deoarece acțiunea hormonului luteinizant se efectuează la nivelul lor (Ryan, 1969).
Conversia acetatului în colesterol are loc în fracțiuni celulare solubile și microsomale, iar colesterolul în pregnenolonă apare în fracțiuni mitocondriale.
Formarea gestagenelor
Conversia pregnenolonei în progesteron poate fi efectuată și în toate organele endocrine care sintetizează steroizi, cu toate acestea, datorită specificității sistemelor enzimatice, aceasta predomină în corpul galben și parțial în foliculi. Progesteronul este secretat nemodificat sau, datorită reducerii cetonelor 20-progesteron în grupa 20a-hidroxil a metabolitului, este transformat într-un alt progestogen activ - 20a-oxipregn-4-en-3-one (Dorfman și Ungar, 1965) .
O conversie suplimentară a pregnenolonului poate avea loc atât prin progesteron, cât și prin hormoni androgenici, ceea ce este ilustrat de schema de mai jos (conform lui Ryan, 1961).
Formarea androgenilor are loc în principal „în testicule, dar și în glandele suprarenale, foliculii, corpul galben sau stroma ovariană prin 17-hidroxilare a pregnenolonului sau progesteronului (Dorfman, 1962; Ryan, 1965, 1969).
Reacțiile de formare a compușilor 17-hidroxi apar în fracția microsomală a celulelor, în timp ce reacția dehidrogenază, inclusiv conversia testosteronului și a androstendionei, are loc într-un sistem enzimatic solubil.
Androstendiona sintetizată este secretată de ovar, care se pare că este principala sursă a acestui steroid în sângele femeilor.
Formarea estrogenului
Estrogenii se formează din androstendionă sau testosteron în timpul reacției de aromatizare (formarea a trei legături nesaturate în inelul steroid A), care are loc în fracțiunile de celule microsomale (Ryan, 1963). Această reacție poate apărea în stroma, stratul cortical, celulele hilus și granuloase ale ovarului, în folicul, corpul galben și, de asemenea, într-un anumit volum în glandele suprarenale și testicule.
Există mai multe căi pentru biosinteza estrogenilor. Astfel, estradiolul poate fi format din testosteron, iar estrona din androstendionă. În plus, estradiolul și estrona sunt interconvertite datorită acțiunii enzimei steroid dehidrogenază, care este prezentă în multe țesuturi ale corpului. Estriolul este sintetizat în ovare și ca urmare a metabolismului estronei și estradiolului - în ficat și în alte organe.
Biosinteza hormonilor steroizi apare sub acțiunea unor sisteme enzimatice foarte specifice. Dar, deoarece căile individuale pentru formarea progesteronului, androgeni și estrogeni sunt strâns interconectate, iar abilitățile biosintetice ale țesuturilor producătoare de hormoni coincid în mare măsură, formarea predominantă a unuia sau a altui hormon depinde de localizarea enzimelor. Deci, în biosinteza tuturor steroizilor sexuali, un rol important revine 3 | 3-ol-steroid dehidrogenazei, care transformă pregnenolona în progesteron. Această enzimă se găsește în multe organe endocrine, astfel încât primele etape ale steroidogenezei pot apărea atât în ovare, cât și în cortexul suprarenal. Etapele ulterioare ale formării de androgeni, gestageni și estrogeni, datorită localizării diferite a enzimelor, se desfășoară în principal într-unul sau alt organ endocrin.
Existența unei căi comune de metabolism și biosinteza hormonilor steroizi explică, de asemenea, faptul că în fiecare glandă care produce steroizi, se formează, de asemenea, cantități mici de alți hormoni din acest grup. Deci, în glandele suprarenale se produc cantități mici de estrogeni pe lângă ovare, se formează progesteron, pe lângă corpul galben, în folicul și glandele suprarenale și androgeni în ovare și glandele suprarenale.
Întreruperea metabolismului hormonilor steroizi din glandele endocrine, adesea asociată cu modificări enzimatice, poate duce la acumularea în organism a substanțelor care sunt produse intermediare ale biosintezei și sunt de obicei prezente doar în cantități mici. Deci, lipsa enzimelor care transformă androgeni în estrogeni (enzime de aromatizare) poate provoca o creștere accentuată a androgenilor în corpul unei femei și apariția sindromului viril. Deficitul de enzime (D5,3 | 3-ol-steroid dehidrogenaza, care acționează în stadiul transformării pregnenolonei în progesteron, precum și enzimele aromatizante implicate în conversia androstendionei și testosteronului în estrogeni) pot servi ca o posibilă cauză de apariție ( EA Bogdanova, 1969) ...
Faptul că androgenii sunt precursori ai estrogenilor pe calea biosintezei estrogenilor este confirmat de numeroase date experimentale și clinice. În experimentele cu incubarea secțiunilor de țesut ale placentei și ovarelor cu hormoni androgenici marcați cu carbon, s-a arătat conversia androstendionei în estronă. În clinică, în tratamentul cancerului de sân cu doze masive de androgeni (propionat de testosteron), s-a constatat o ușoară creștere a excreției de estrogen.
Reduceți sinteza (inhibă transcripția) prolactostatina (este dopamina). Stimulați secreția iritarea sfarcurilor în timpul alăptării, sarcinii, frecvență crescută a contactelor sexuale, stres, somn, serotonină, estrogeni, angiotensină
Reduce secreția dioxifenilalaninei (DOPA).
Mecanism de acțiune
Necunoscut sigur. Există dovezi ale prezenței unei peptide mesager secundare M-1500, care stimulează sinteza cazeinogenului.
Ținte și efecte
În rinichi, împreună cu hormonul paratiroidian și hormonul de creștere, stimulează hidroxilarea și activarea vitaminei D.
o stimulează creșterea sânilor și alăptarea în prezența unor niveluri suficiente de hormoni sexuali feminini, corticosteroizi și insulină,
o în timpul sarcinii susține activitatea corpului galben și secreția de progesteron, o mărește sinteza cazeogenului ARN, lactozei sintază și ADN,
o participă la menținerea instinctului matern.
o în celulele Leydig crește sinteza testosteronului, o stimulează prostata și secreția acesteia,
o potențează efectul LH și FSH asupra spermatogenezei și a activității spermatozoizilor.
Patologie
Hipofuncţie
Sindromul Sheehan - un factor de risc este pierderea excesivă de sânge în timpul nașterii, ceea ce duce la afectarea alimentării cu sânge și a necrozei hipofizare. Primul semn este încetarea alăptării, apoi se găsesc alte simptome ale hipopituitarismului.
Cauza hiperfuncției. Sinteza excesivă apare cu hipotiroidismul, producător de hormoni
tumori, insuficiență renală cronică.
Tabloul clinic. Ca urmare, infertilitatea se dezvoltă la bărbați și femei, impotența și ginecomastia la bărbați, amenoreea și galactoreea la femei.
Creșterea nivelului hormonal în timpul lactației postpartum are un efect anovulator mic asupra ovarelor, care poate reduce probabilitatea de sarcină.
G HORMONI ONADOTROPICI
Acestea includ hormonul foliculostimulant (FSH) și hormonul luteinizant (LH)
noi, coriogonina umană.
Structura
FSH și LH sunt glicoproteine cu o greutate moleculară de 30 kDa. Choriogonina, un hormon placentar, este, de asemenea, o glicoproteină. Toți acești hormoni sunt co-
Sunt formate din subunități α și β, subunitatea β a fiecărui hormon este individuală, subunitatea α este aceeași și similară cu subunitatea α a hormonului stimulator al tiroidei.
Sinteză
Se efectuează în gonadotrofele hipofizare.
Reglarea sintezei și secreției
Gonadoliberina activează sinteza și secreția în unde cu un ciclu de aproximativ 90 ".
Reduceți sinteza endorfinelor și a hormonilor sexuali indirect prin suprimarea sintezei gonadoliberinei. Hormonii sexuali, în funcție de concentrația lor, suprimă direct secreția acestor hormoni.
Mecanism de acțiune
Adenilat ciclază.
Ținte și efecte
La bărbați, hormonul luteinizant
o în celulele Leydig crește sinteza colesterolului și a testosteronului suplimentar.
Avea femeia hormon luteinizant
o în corpul galben crește sinteza colesterolului, progesteronului și androgenilor,
o ca urmare a creșterii concentrației dependente de estradiol determină inducerea ovulației.
Patologie
Hipofuncţie
Hormonul foliculostimulant
o stimulează creșterea tubulilor seminiferi, a testiculelor, inițiază sperma
o acționează asupra celulelor Sertoli ale testiculelor și crește sinteza proteinelor care leagă androgenii, ceea ce asigură absorbția testosteronului din sânge și transportul testosteronului către canalele deferente și epididimul. Acest lucru vă permite să creșteți concentrația de testosteron în această zonă și să stimulați spermatogeneza.
Hormonul foliculostimulant
o activează creșterea foliculilor și îi pregătește pentru acțiunea LH,
o îmbunătățește conversia androgenilor în estrogeni.
o pubertate târzie apare la copii,
o la femei - oligomenoree, lipsa ovulației și infertilității, atrofia glandei mamare și a organelor genitale,
o la bărbați - impotență, azoospermie, atrofie testiculară,
o la ambele sexe - scăderea libidoului, creșterea părului corporal, subțierea pielii și a ridurilor acesteia.
Hiperfuncție
O creștere a FSH duce adesea la sângerări uterine disfuncționale.
Hormoni gonadotropi sunt sintetizate în hipofiza anterioară. În general, hormonii glandei pituitare anterioare controlează și stimulează toate glandele endocrine ale corpului. Glanda pituitară este stimulată de neurohormonii glandei pineale și hipotalamusului. Luați în considerare efectul hormonilor gonadotropi asupra organelor de reproducere (genitale) ale corpului feminin.
Hormonul foliculostimulant hipofizar(FSH) promovează maturarea foliculului și producția foliculară. Hormonul luteinizant (LH) stimulează dezvoltarea corpului galben și hormonul luteotrop LTG(prolactină, mamotropină) - secreția hormonului corpului galben (). FSH și LH sunt sintetizate simultan în hipofiza anterioară, dar în diferite rapoarte: în prima jumătate a ciclului predomină FSH, în a doua jumătate - LH, precum și LTH.
Hormonii gonadotropi ai hipofizei afectează endometrul prin ovar. Hormonii foliculului și corpul galben, formați sub influența hormonilor gonadotropi ai hipofizei, cauzează (hormonul folicular - proliferare, hormonul corpului galben - secreția). Hormonii gonadotropi nu au un efect direct asupra endometrului.
Nu există o legătură unidirecțională între glanda pituitară anterioară și ovare, ci o interacțiune complexă prin hipotalamus. Glanda pituitară, care stimulează funcția ovarelor, este la rândul ei influențată (prin hipotalamus) de hormonii foliculului și corpul galben.
Producția crescândă de hormon folicular (în foliculul maturizant) inhibă secreția hormonului foliculostimulant hipofizar (FSH). Acest lucru crește secreția de hormon luteinizant (LH), care este necesară pentru ovulație și, în continuare, pentru dezvoltarea corpului galben. Secreția crescută a hormonului corpului galben întârzie formarea LH. O scădere a secreției acestui hormon duce la o creștere a secreției de FSH, în legătură cu care începe un nou ciclu în ovar.
Astfel, există o creștere a secreției de FSH, apoi a LH: o schimbare periodică a hormonilor gonadotropi, la rândul ei, cauzează.
Interacțiunea hormonilor glandei pituitare și a ovarului se realizează prin sistemul nervos, în special cu ajutorul centrelor autonome din regiunea hipotalamică.
În timpul sarcinii, o nouă sursă puternică de secreție a hormonilor gonadotropi apare în corpul unei femei - corionul. Deja în primele săptămâni de sarcină se formează o cantitate mare de gonadotropină corionică, care are un efect luteinizant. După formarea placentei, hormonul gonadotrop se formează în mucoasa epitelială a vilozităților (în citotrofoblast). Gonadotropina corionică intră în fluxul sanguin al gravidei și este excretată în urină. Metodele pentru diagnosticarea precoce a sarcinii se bazează pe această proprietate a urinei gravidelor. După a patra lună de sarcină, activitatea gonadotropă a placentei scade. După naștere, eliberarea hormonilor gonadotropi scade brusc și după 10-15 zile nu sunt detectate în urină.
În corpul unei femei care se pregătește să poarte și să nască un copil, fundalul hormonal se schimbă în primele săptămâni. Unul dintre cei mai importanți markeri ai acestei perioade este hCG - gonadotropina corionică umană. Odată cu insuficiența sa, există întârzieri în dezvoltarea organelor și țesuturilor embrionului, poate apărea hipoxie intrauterină. Acest lucru duce la necesitatea obținerii hormonului din exterior, pentru care medicii prescriu injecții cu medicamentul cu același nume. Cum funcționează și în ce alte situații este necesar?
Ce este gonadotropina corionică
Când ovulul se atașează de perete, țesutul corionic (membrana ovulului, parte a placentei) începe să sintetizeze hormonul gonadotrop, a cărui creștere a nivelului este un semnal pentru debutul sarcinii (nu fertilizarea) - după că începe dezvoltarea embrionului. Principalele caracteristici ale gonadotropinei corionice umane:
- Aparține categoriei hormonilor gonadotropi, este legat de hormonul luteinizant (LH) și hormonul foliculostimulant (FSH), conține 237 de aminoacizi.
- Se produce deja în primele ore de sarcină, vârful de sinteză (nivel maxim) se observă la 7-11 săptămâni.
- În ceea ce privește structura chimică, este o glicoproteină formată din subunități alfa și beta. Acesta din urmă este unic, iar subunitatea alfa o face legată de LH, FSH și TSH (hormonul stimulator al tiroidei, produs de glanda tiroidă).
- La femeile sau bărbații care nu sunt gravide, se observă o creștere a nivelului de gonadotropină corionică în prezența neoplasmelor care o sintetizează (tumori ale sistemului reproductiv).
Toate testele de sarcină utilizate acasă măsoară nivelul hCG în urină. Pentru a compensa lipsa gonadotropinei corionice, a fost creat un medicament cu același nume. Acest medicament este prescris exclusiv de un medic pe baza rezultatelor testelor.
Compoziţie
Pachetul de medicamente conține 2 fiole cu conținut diferit. Baza principalului medicament (pulbere liofilizată) este hormonul cu același nume - gonadotropina corionică, a cărei concentrație poate fi (în UI):
- 1000;
- 1500;
- 5000.
Substanța este obținută prin extracția (excreția) din urina femeilor însărcinate și purificarea ulterioară, prin urmare hormonul este complet natural pentru corpul uman. Un element suplimentar în compoziția pulberii este manitol (manitol), a cărui cantitate pentru toate dozele de ingredient activ este de 20 mg. Solventul conținut în a doua sticlă este o soluție izotonică de clorură de sodiu (0,9%).
Eliberați formularul
Gonadotropina corionică în farmacii se găsește exclusiv sub forma unui liofilizat - o pulbere albă obținută printr-o metodă inovatoare de uscare moale (deshidratare prin congelare și uscare în vid). Avantajul acestei forme este depozitarea pe termen lung, absența unor cerințe stricte pentru condițiile de temperatură a aerului din jur. Liofilizatul de hCG este închis în flacoane tubulare de sticlă. Pentru 1 pachet de carton al medicamentului există 5 fiole cu liofilizat, suplimentate cu fiole similare pentru diluare (1 ml fiecare).
efect farmacologic
Gonadotropina corionică aparține grupului de hormoni ai hipotalamusului, hipofizei, gonadotropinelor și antagoniștilor acestora, are efect luteinizant, foliculostimulant și gonadotrop. Efectul luteinizant este mai pronunțat decât cel al LH în sine, sintetizat de hipofiza anterioară. Efectul specific asupra corpului depinde de sexul persoanei. La femei, hormonul gonadotrop este responsabil de:
- menținerea dezvoltării normale, complete a placentei care înconjoară fătul;
- stimularea sintezei progesteronului de către corpul galben;
- ruperea foliculului și inhibarea debutului fazei menstruale;
- activitate funcțională crescută a corpului galben în faza luteală a ciclului menstrual;
- sinteza estrogenilor (și a androgenilor slabi) de către aparatul folicular al ovarelor, în special în caz de insuficiență a corpului galben;
- stimularea și inducerea (îmbunătățirea) procesului de ovulație.
La ambele sexe, gonadotropina corionică este cel mai important element responsabil de maturarea gametilor (spermatozoizii și ovulelor), de creșterea corectă a acestora și de sinteza hormonilor sexuali. La bărbați, datorită acestui hormon:
- crește producția de dihidrotestosteron și testosteron;
- spermatogeneza crescută (dezvoltarea spermei);
- stimulează activitatea celulelor testiculare Leydig;
- testiculele coboară în scrot (în prezența criptorhidiei - locația testiculelor în afara scrotului).
În plus, gonadotropina corionică este responsabilă pentru dezvoltarea caracteristicilor sexuale secundare și a organelor sistemului reproductiv la bărbați și femei. Medicii sugerează că are și proprietăți corticotrope, afectând steroidogeneza în cortexul suprarenal. Acest lucru duce la o creștere a secreției de hormoni glucocorticoizi și adaptează corpul feminin la sarcină, care este percepută ca stres.
Indicații de utilizare
Femeilor li se recomandă să efectueze administrarea intramusculară de gonadotropină corionică dacă au diagnosticate următoarele probleme:
- amenoree, dismenoree (durere în timpul sângerării, nereguli menstruale);
- sângerări uterine disfuncționale (dacă femeia nu se află în menopauză);
- disfuncție ovariană anovulatorie (și infertilitatea rezultată);
- insuficiența corpului galben (când funcția estrogenică a ovarelor este normală);
- avort;
- riscul avortului spontan în primul trimestru.
Medicul poate prescrie un hormon pentru menținerea fazei corpului galben în timpul tehnicilor de reproducere asistată (ca mijloc de stimulare a ovulației, atunci când foliculii sunt pregătiți pentru puncție). Dacă vorbim despre gonadotropină pentru bărbați, aceștia au indicații pentru utilizarea acesteia: hipogonadism (secreție insuficientă de androgeni, o formă de infertilitate), inclusiv pregătirea pentru testul Leydig înainte de a prescrie medicamente stimulante;
- pubertate întârziată;
- oligoastenospermia (abateri în densitatea și structura spermei de la normă), azoospermia (absența spermei în ejaculat);
- testarea criptorhidiei sau anorhismului (băieți);
- infantilismul sexual (subdezvoltarea sistemului reproductiv);
- hipogenitalism;
- sindrom adiposogenital.

Instructiuni de folosire
Pentru a obține produsul, pulberea se amestecă cu un solvent și se agită bine. Injecția intramusculară se efectuează lent. Compilarea și corectarea schemelor terapeutice se efectuează de către un medic. O concentrație ridicată de hormon (5000 UI) este utilizată la femei după transferul de embrioni timp de 9 zile de până la 3 ori (interval 2-3 zile, doză - 1500-5000 UI). Gonadotropina corionică 1000, 1500 sau 500 UI se utilizează după cum urmează:
| Indicații | Dozare, în UI | Schema de utilizare |
|---|---|---|
| Funcția insuficientă a corpului galben | În fiecare zi, din ziua ovulației până în momentul menstruației potențiale sau înainte de sarcină |
|
| Stimularea ovulației (pe fondul inseminării artificiale) | O dată la două zile, la sfârșitul finalizării terapiei cu hormoni foliculostimulanți, o dată |
|
| Cicluri anovulatorii | De 3 ori în 9 zile, începând cu a 10-a zi a ciclului menstrual |
|
| Avort | 5000 (10000 UI în prima zi) | De la 8 la 14 săptămâni de gestație zilnic |
| Bărbați (băieți) |
||
| Hipogonadism hipogonadotrop | Cu o frecvență de până la 3 r / săptămână, timp de 3 luni |
|
| Stimularea spermatogenezei (cu infertilitate) | ||
| Pubertate întârziată | Cu o frecvență de până la 3 r / săptămână, timp de șase luni |
|
| Criptorhidism | Cu o frecvență de până la 3 r / săptămână, efectuați 10 proceduri |
|
| Identificarea hipogonadismului la adolescenți | Zilnic timp de 3 zile |
|
Cum să luați în culturism
La sfârșitul anului 2011, suplimentele alimentare care conțin hCG au fost interzise oficial în Statele Unite, deoarece studiile (și recenziile sportivilor) nu au arătat niciun efect din utilizarea hormonului în această formă. Injectabil, gonadotropina în culturism este utilizată ca mijloc de creștere a secreției de testosteron, eliminând unele dintre efectele secundare ale steroizilor anabolizanți și păstrând masa musculară. Dozare - de la 4000 UI pe săptămână, există mai multe opțiuni de utilizare:
- Când utilizați steroizi anabolizanți într-un regim pe termen lung (de la 6 săptămâni): 2 r / săptămână injectați 250-500 UI de gonadotropină.
- Terapia cu steroizi post-ciclu: injectați 2.000 UI la fiecare două zile timp de 3 săptămâni.
- Utilizarea continuă a steroizilor: doză individuală, utilizare timp de 5 săptămâni și pauză timp de 14 zile.
Aplicare în timpul sarcinii și alăptării
Perioada de lactație este o contraindicație pentru utilizarea gonadotropinei corionice. Dacă medicul consideră că este necesar să se efectueze terapia hormonală, copilul este înțărcat pe toată durata cursului. Sarcina se numără, de asemenea, printre contraindicațiile medicamentului, dar dacă apare ca urmare a utilizării unui hormon, reanumirea este permisă până la a 10-a săptămână, conform indicațiilor medicului. Nu este exclus un efect negativ al hormonului asupra fătului, avortului spontan sau apariția sarcinilor multiple pe fondul tratamentului de lungă durată cu gonadotropine.
Supradozaj
Toxicitatea medicamentului este scăzută, dar dacă terapia cu gonadotropină corionică a fost efectuată la începutul ciclului menstrual și a fost caracterizată prin introducerea unor doze mari, se poate dezvolta sindromul de hiperstimulare ovariană. Se pare astfel:
- durere abdominală ușoară, disconfort;
- o creștere a chisturilor ovariene, o creștere a sensibilității (la durere) a glandelor mamare;
- greață, vărsături, diaree;
- simptome clinice și semne de ascită la ultrasunete;
- greutate corporală crescută.
Dacă apar semne de supradozaj, este necesară anularea temporară a gonadotropinei, efectuarea tratamentului simptomatic. Include multă băutură, odihnă la pat, normalizarea echilibrului apă-sare. Dacă starea pacientului este gravă, sunt necesare spitalizarea și observarea în spital. La bărbați, o supradoză de hormon hCG duce în principal la:
- tulburări de comportament sexual (la băieți);
- ginecomastie;
- degenerarea glandelor sexuale;
- scăderea numărului de spermatozoizi în ejaculare.

Efecte secundare
Sistemul endocrin reacționează predominant la tratamentul cu gonadotropină la persoanele de ambele sexe;
- mărirea testiculelor în canalul inghinal, pubertatea mai timpurie, atrofia tubulilor seminiferi (pentru bărbați);
- formarea anticorpilor împotriva hormonului;
- edem periferic, formarea chisturilor ovariene, mărirea sânilor, sindromul de hiperstimulare ovariană (pentru femei);
- durere de cap;
- răspuns alergic (umflături, senzație de arsură, roșeață),
- depresie.
Contraindicații
Conform instrucțiunilor oficiale, există mai multe tipuri de contraindicații pentru gonadotropina corionică. Relativ - hormonul poate fi prescris în doze reduse sau într-un curs scurt și întotdeauna sub supravegherea unui medic, dacă pacientul are:
- astm bronsic;
- insuficiență cardiacă, hipertensiune;
- afectarea funcției renale;
- epilepsie;
- risc crescut de tromboză (pe fondul trombofiliei, obezității severe, transmisiei ereditare).
Băieților în vârstă pre-pubertară li se prescrie un hormon numai atunci când este urgent nevoie. Contraindicațiile absolute afectează femeile:
- hipertrofie hipofizară;
- prezența oricăror tumori maligne de natură dependentă de hormoni care afectează organele sistemului reproductiv, glanda mamară (suspiciunea prezenței lor este, de asemenea, o contraindicație), în special cancer (uter, ovar, sân, prostată), carcinom mamar (pentru bărbați);
- hipotiroidism (producție în exces de hormoni tiroidieni);
- hiperprolactinemie (exces de prolactină în sânge);
- leziuni ale sistemului nervos central care afectează hipotalamusul sau hipofiza (neoplasme);
- insuficiență suprarenală;
- tromboflebită venoasă profundă;
- insuficiență ovariană primară;
- sângerări vaginale și uterine de etiologie necunoscută;
- tumoare fibroasă a uterului (cu incompatibilitate constatată cu sarcina);
- sindromul ovarului polichistic, antecedente de hiperstimulare ovariană (dozele mari sunt interzise - 5000 UI);
- infertilitate neasociată cu anovulație;
- hernie inghinală (la bărbați);
- obstrucția trompelor uterine;
- pubertate mai timpurie;
- vârsta copiilor până la 3 ani.
Analogi
Toți analogii conțin un hormon gonadotropic obținut în mod natural, diferă în principal prin prețul și concentrația substanței active:
- Corala;
- Ecostimulină;
- Horagon;
- Profazi;
- Pregnil.

Preț
Prețuri aproximative pentru diferite farmacii și opțiuni de medicamente (5 perechi de fiole):
| Concentraţie | Zdravzona | |
|---|---|---|
| 500 UI | ||
| 1000 UI | ||
| 1500 UI |
Video
Hormonii sunt substanțe organice cu structuri diferite care pot afecta activitatea vitală a corpului uman. Hormonii gonadotropi afectează funcționarea sistemului reproductiv. Sunt sintetizate în lobul anterior al hipofizei și de acolo sunt secretate în sânge.
Hormonii glandei pituitare anterioare
Glanda pituitară este împărțită în doi lobi: anterior și posterior. În față, hormonii sunt sintetizați direct și eliberați în sânge. În lobul posterior al hipofizei, acestea provin din hipotalamus și sunt secretate în sânge numai în anumite circumstanțe.
Hormonii gonadotropi ai hipofizei stimulează activitatea glandelor sexuale. Acestea includ:

Producția de hormoni se efectuează în gonadotropele (celulele bazofile) ale adenohipofizei. Ele reprezintă aproximativ 15% din toate celulele lobului anterior.
Hormonul sarcinii - hCG
În timpul fertilizării și implantării ovulului în peretele uterului, corpul femeii începe să producă hormoni gonadotropi hipofizari specifici, reprezentați de gonadotropina corionică.

Funcțiile hormonului includ menținerea corpului galben (secreția de estrogen și progesteron) până când placenta este complet coaptă. Are un efect luteinizant ridicat asupra corpului, care este în mare măsură superior FSH și LH.
Caracteristicile structurale ale hormonilor
Activitatea biologică a hormonilor este asigurată de structura lor unică, care include două subunități. Prima, o subunitate, are o structură aproape identică pentru toți hormonii gonadotropi, în timp ce subunitatea b oferă unicitatea acțiunii hormonului.

În mod individual, aceste subunități nu au niciun efect asupra corpului, dar atunci când se combină, este asigurată activitatea lor biologică și influența asupra proceselor vitale ale corpului, în special sistemul reproductiv. Astfel, hormonii gonadotropi au un efect important nu numai asupra sferei sexuale, ci și asupra proceselor endocrine și asupra reglării echilibrului hormonal.
Cum afectează hormonii corpul
Încă din cele mai vechi timpuri, oamenii de știință au căutat să studieze activitatea biologică a hormonilor și efectul acestora asupra corpului uman. Hormonii gonadotropi au o mare influență asupra proceselor vitale ale corpului uman. Prin urmare, studiul mecanismului acțiunii lor este o problemă foarte importantă și interesantă. Când s-au efectuat studii cu hormoni marcați, a fost posibil să se stabilească faptul că celulele sunt capabile să recunoască un anumit hormon și să se lege numai de anumite celule.
Procesul de legare la o celulă se realizează prin prezența în membrană sau în interiorul celulei în sine a unei molecule proteice - un receptor. Recepția intracelulară se referă la hormonii steroizi, deoarece aceștia tind să pătrundă în celulă și să afecteze activitatea acesteia. Recepția membranei este inerentă în care se leagă de membrana membranară a celulei.
Legarea hormonului de proteina receptorului contribuie la formarea complexului. Această etapă are loc fără participarea enzimelor și este reversibilă. Hormonii steroizi intră în celulă și se leagă de receptor. După transformare, complexul format pătrunde în nucleul celular și promovează formarea de ARN specific, în citoplasma căruia sunt sintetizate particule enzimatice, care determină efectul hormonilor asupra celulei.
Hormoni gonadotropi: funcții și influență asupra proceselor sistemului reproductiv
FSH este cel mai activ la femei. Stimulează creșterea celulelor foliculare, care, sub influența GSIC, se transformă în vezicule și se maturizează până la stadiul ovulației.
Sub influența FSN, se observă o creștere a masei ovarelor și a testiculelor. Cu toate acestea, chiar și cu introducerea artificială a unui hormon sintetic, este imposibil să se inducă dezvoltarea țesutului interstițial, care afectează secreția de androgeni testiculari.

GSIK este responsabil pentru ovulație și formare și, împreună cu acesta, afectează secreția de estrogen. Sub influența unui hormon care stimulează celulele interstițiale, organele responsabile de caracteristicile sexuale secundare cresc.
Acțiunea biologică a LTG
LTH este foarte asemănător cu hormonul de creștere. După efectuarea studiilor de laborator, s-a descoperit că se află într-o singură moleculă, prin urmare, fiecare dintre acești hormoni nu poate fi izolat separat la om. Funcțiile LTG includ secreția de lapte și progesteron. Este important de menționat aici că aceste procese sunt determinate de interacțiunea unui număr mare de hormoni, deoarece atunci când numai LTG este expus corpului, aceste funcții nu se manifestă.
Deci, sunt necesari următorii hormoni pentru a excreta laptele:
- FSH și GSIK - provoacă secreția de estrogen în ovare;
- sub influența STH și a estrogenilor, apare creșterea canalelor de lapte;
- LTH induce secreția de progesteron în corpul galben;
- progesteronul stimulează dezvoltarea deplină a glandei mamare la nivel alveolar-lobular.
Hormonii gonadotropi necesită o interacțiune regulată pentru a asigura întreaga activitate a corpului și a tuturor sistemelor sale. De aceea, influența separată a fiecăruia dintre ei (în cazul introducerii hormonilor sintetici) nu provoacă reacția așteptată a corpului.
Hormonul hipotalamic
Hipotalamusul secretă hormonul care eliberează gonadotrop în sânge. Are o structură polipeptidică și afectează secreția de hormoni hipofizari. Într-o măsură mai mare, afectează hormonul luteinizant și apoi hormonul foliculostimulant. GnRH este produs la intervale de timp bine definite, la femei variază de la 15 la 45 de minute (în funcție de ciclu), iar la bărbați hormonul este secretat la fiecare 90 de minute.

Odată cu introducerea artificială a unui hormon sintetic prin picurare, funcțiile secreției hormonale sunt întrerupte, care constau într-o creștere pe termen scurt a secreției și apoi într-o încetare completă a producției de hormoni gonadotropi de către glanda pituitară anterioară.
Procesul de expunere la gonadoliberină pe corp
GnRH stimulează lobul hipofizar anterior, ale cărui celule (gonadotropine) au un receptor specific de gonadoliberină pentru secretarea hormonilor foliculostimulatori și luteinizatori, care, la rândul lor, afectează funcționarea gonadelor.

FG stimulează maturarea spermei și a ouălor, LH afectează secreția de hormoni sexuali (estrogen, progesteron, testosteron). Sub influența hormonilor sexuali, celulele se maturizează și devin gata de fertilizare.
Cu un curs excesiv de rapid al proceselor de ovogeneză și spermatogeneză, se eliberează inhibină, care afectează hormonii gonadotropi ai lobului anterior al hipofizei, care încetinește maturarea celulelor germinale acționând asupra hormonului foliculostimulant.
La ce se utilizează medicamentele gonadotrope?
Tot mai des în practica medicală, tratamentul se găsește prin introducerea hormonilor artificiali. Pentru unele boli endocrine sau tulburări ale sistemului reproductiv uman, se utilizează preparate de hormoni gonadotropi. Introducerea lor, într-o anumită măsură, are un efect asupra producției de hormoni sexuali și asupra proceselor care au loc în organism.
În cazul unei încălcări a sintezei hormonilor gonadotropi, se pot dezvolta anumite tulburări endocrine (avorturi spontane în primul trimestru, imaturitate sexuală, infantilism sexual, boala Simmonds și sindromul Sheehan).
Pentru a neutraliza aceste patologii, se efectuează un test de sânge și o analiză a compoziției sale hormonale. Apoi sunt prescrise medicamente, care sunt necesare pentru a restabili echilibrul corect al hormonilor și, în consecință, reglarea proceselor vitale din organism.